Theo thông tin mới đây, Cục Quản lý Dược đã có ý kiến về thủ tục nhập khẩu lô thuốc Tasigna - thuốc đặc trị ung thư bị chậm trễ.
Tin nên đọc
 Bài thuốc thần kỳ chữa ung thư di căn, đặc trị khối u bướu
Bài thuốc thần kỳ chữa ung thư di căn, đặc trị khối u bướu
 Tiêu hủy 20.000 viên thuốc trị ung thư: Tiết lộ bất ngờ của Hải quan
Tiêu hủy 20.000 viên thuốc trị ung thư: Tiết lộ bất ngờ của Hải quan
 Vì sao gần 20.000 viên thuốc đặc trị ung thư, trị giá gần 14 tỷ đồng bị tiêu huỷ
Vì sao gần 20.000 viên thuốc đặc trị ung thư, trị giá gần 14 tỷ đồng bị tiêu huỷ
 Cô giáo mắc bệnh ung thư giai đoạn cuối vẫn lên lớp đều đặn
Cô giáo mắc bệnh ung thư giai đoạn cuối vẫn lên lớp đều đặn
Nhập thuốc trậm chễ không phải do thủ tục hải quan
Ngày 8/5 Bộ Tài Chính cũng đã có thông tin chính thức về thủ tục nhập khẩu lô thuốc bị chậm trễ không phải do không phải do cơ quan hải quan kéo dài thời gian làm thủ tục.
Theo Tổng cục Hải quan, lô hàng nêu trên là thuốc Tasigna (nilotinib) 200mg viên nang cứng, số lượng 309 hộp, mỗi hộp 112 viên, hạn dùng 24 tháng, sản xuất tháng 6/2013 và hết hạn tháng 5/2015. Lô hàng do Tổ chức Novatis Pharma AG trao tặng cho Bệnh viện Truyền máu huyết học TP HCM.
Theo giải trình của Bệnh viện đã có công văn gửi Cục Quản lý dược (Bộ Y tế) đề nghị được tiếp nhận lô hàng. Tuy nhiên, ngày 12/12/2013, Cục Quản lý dược có công văn trả lời không đồng ý để bệnh viện tiếp nhận lô hàng do thiếu văn bản phê duyệt của cơ quan có thẩm quyền và một số loại chứng từ.
Sau khi Bệnh viện giải trình, ngày 14/7/2014, Cục Quản lý dược có công văn đồng ý để bệnh viện tiếp nhận lô hàng, trong đó yêu cầu: Hạn dùng còn lại kể từ ngày cập cảng Việt Nam không được dưới 12 tháng.
Theo vận đơn, lô hàng tính từ thời điểm cập cảng Việt Nam ngày 23/7/2014, hạn dùng còn lại của thuốc không đủ 12 tháng.
Sau khi Bệnh viện có công văn gửi Cục Hải quan TP HCM giải trình và xin được thông quan vì lý do nhân đạo, cơ quan hải quan đã tiếp nhận làm thủ tục ngay cho 2 tờ khai hải quan nhập khẩu thuốc viện trợ. Thời gian thông quan lô thuốc này được giải quyết trong 1 ngày.
Như vậy, việc số thuốc quá hạn dùng bị tiêu hủy do cơ quan chức năng thực hiện theo quy định hiện hành và không phải do cơ quan hải quan kéo dài thời gian thông quan.
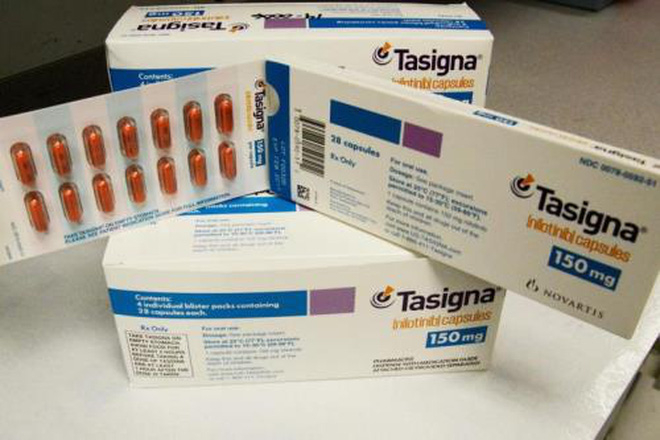 |
| Gần 20.000 viên thuốc đặc trị ung thư bị tiêu hủy vì quá hạn. Ảnh: minh họa |
Cục Quản lý Dược cấp phép nhập khẩu thuốc theo đúng quy định
Tối cùng ngày, Cục Quản lý Dược đã có ý kiến về sự việc trên. Theo đó, ngày 3/5/2017, Cục Quản lý Dược tiếp nhận từ các phương tiện thông tin, truyền thông về việc 20.000 viên thuốc Tasigna điều trị ung thư được tài trợ từ Công Novartis bị tiêu hủy do hết hạn dùng.
Cùng ngày, Cục Quản lý Dược đã có Công văn hỏa tốc số 6110/QLD-KD gửi Sở Y tế TP HCM yêu cầu báo cáo khẩn vụ việc trên. Báo cáo yêu cầu gửi về Vụ Bảo hiểm y tế và Cục Quản lý Dược, Bộ Y tế trước ngày 7/05/2017. Tuy nhiên đến nay (ngày 08/05/2017), Cục Quản lý Dược vẫn chưa nhận được báo cáo từ Sở Y tế TP HCM.
Về phía Cục quản lý Dược, việc cấp phép nhập khẩu thuốc Tasigma đã được thực hiện đúng theo quy định tại khoản 2 Điều 16 Thông tư 47/2010/TT-BYT hướng dẫn hoạt động xuất khẩu, nhập khẩu thuốc và bao bì tiếp xúc trực tiếp với thuốc và đáp ứng quy định về thời gian không quá 15 ngày làm việc, cụ thể:
- Ngày 28/11/2013, Bệnh viện Truyền máu huyết học (TMHH) TP HCM có Công văn số 1639/TMHH-KHTC gửi Cục Quản lý Dược đề nghị tiếp nhận thuốc Tasigna do Công ty Novartis Pharma viện trợ.
- Ngày 12/12/2013, căn cứ điểm c khoản 1 Điều 16 Thông tư 47/2010/TT-BYT, yêu cầu trong hồ sơ phải có văn bản của cơ quan có thẩm quyền về việc cho phép cơ sở nhận thuốc viện trợ, viện trợ nhân đạo, Cục Quản lý Dược có Công văn số 20956/QLD-KD trả lời BV yêu cầu phải có văn bản của cơ quan có thẩm quyền phê duyệt tiếp nhận viện trợ.
- Ngày 01/07/2014, Bệnh viện có Công văn số 1011/TMHH-KHTH gửi Cục QLD kèm theo Quyết định số 3126/QĐ-UBND ngày 24/6/2014 của UBND TP HCM phê duyệt việc tiếp nhận viện trợ từ Công ty Novartis Pharma.
- Ngày 14/7/2014, Cục Quản lý Dược có Công văn số 11978/QLD-KD đồng ý để Bệnh viện nhận thuốc Tasigna từ Công ty Novartis theo quy định tại Thông tư số 47/2010/TT-BYT trong đó quy định rõ hạn dùng còn lại kể từ ngày cập cảng Việt nam không được dưới 12 tháng
- Ngày 22/8/2014, Bệnh viện có Công văn số 1449/TMHH-KHTH gửi Cục Quản lý Dược đề nghị tiếp nhận thuốc Tasigna có hạn dùng dưới 12 tháng.
Theo Công văn số 1449/TMHH-KHTH, thuốc Tasigna là thuốc điều trị bệnh Bạch cầu mãn dòng tủy thay thế thuốc Glivec sử dụng cho nhiều bệnh nhân đang có tình trạng không dung nạp thuốc Glivec, đồng thời Bệnh viện cam kết sử dụng thuốc Tasigna đúng mục đích và quy định chuyên môn hiện hành.
Căn cứ vào giải trình và cam kết của bệnh viện, ngày 28/08/2014, Cục quản lý Dược có Công văn số 14735/QLD-KD đồng ý cho Bệnh viện tiếp nhận thuốc có hạn dùng dưới 12 tháng lô thuốc Tasigna số lô S0052A hạn dùng tháng 5/2015.
Vậy trách nhiệm thuộc về bên nào khi mà lô thuốc được viện trợ mất tới hơn một năm mới hoàn thành thủ tục nhập thuốc? Liệu sẽ còn những lô thuốc sau đó tiếp tục bị chậm trễ trong quá trình làm thủ tục nhập thuốc?




